자문기구 회의…최종 승인 전 제조공정에 대해서도 승인 받아야
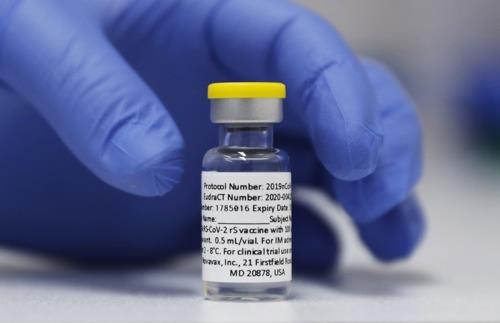
연방 식품의약국(FDA) 자문기구가 7일 노바백스의 신종 코로나바이러스 감염증(코로나19) 백신에 대해 긴급사용을 승인하라고 권고했다.
FDA 자문기구인 백신·생물의약품자문위원회(VRBPAC)는 이날 노바백스의 코로나19 백신에 대해 표결을 실시해 이같이 권고했다고 일간 뉴욕타임스가 보도했다.
노바백스의 백신은 메신저 리보핵산(mRNA) 방식인 화이자·모더나의 백신과 달리 코로나바이러스 표면 단백질로 만들어진 나노입자로 제조됐다.
그는 미국에서는 백신 수용에 문제가 있다면서 생명을 살릴 잠재력을 가진 의약품을 사람들이 받아들이는 것을 좀 더 편안하게 해주는 것이라면 무엇이든 할 필요가 있다고 말했다.
FDA가 관례에 따라 자문기구의 권고를 수용할 경우 노바백스의 백신은 미국에서 성인을 상대로 긴급사용이 승인된 4번째 코로나19 백신이 될 전망이다. 국내에는 이미 도입돼 접종이 이뤄지고 있다.
다만 노바백스는 지난 2년간 거듭해서 백신의 대량생산에 차질을 빚어왔고, 제조 공정과 관련해 FDA의 승인을 먼저 받아야만 하는 상황이라고 NYT는 전했다.
이에 따라 미국에서 노바백스의 코로나19 백신을 실제 접종할 수 있기까지는 여러 주가 더 걸릴 전망이다.
미 보건복지부는 이 백신에 대해 승인이 내려질 경우 제한적인 물량을 받기 위해 연방정부가 노바백스와 조율하고 있다고 밝혔다.
노바백스는 전임 도널드 트럼프 행정부 당시 추진된 신속한 백신 개발·보급 계획인 ‘초고속 작전’에 따라 연방정부의 자금 지원을 받아 백신을 개발했다. 또 승인이 이뤄질 경우 1억1000만회 접종분을 구매하기로 합의했다.
그러나 이미 화이자와 모더나 등 다른 효과 있는 백신이 많이 보급된 만큼 정부는 수백만회 접종분을 구매할 가능성이 높다고 2명의 관계자는 전했다.