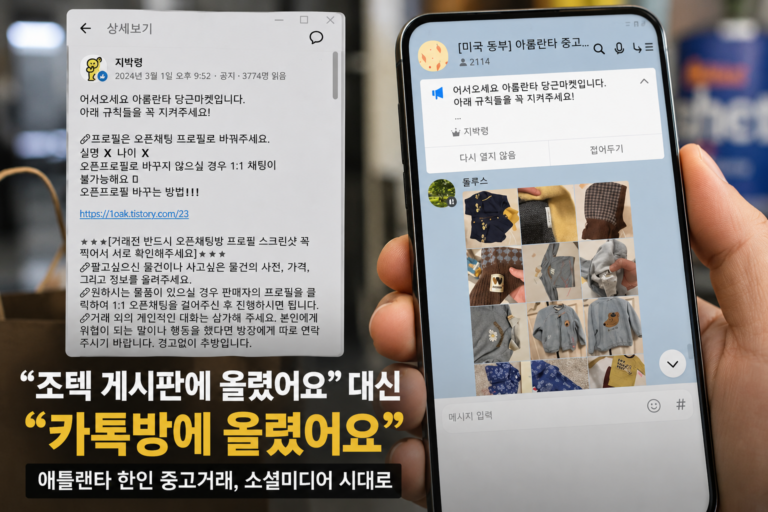
“혈장치료제 안전성 확인”…효과 검증 미비 지적도
연방 식품의약국(FDA)이 23일 신종 코로나바이러스 감염증(코로나19) 혈장치료제의 긴급사용을 승인했다고 로이터통신이 보도했다.
FDA는 이날 성명을 통해 코로나19 혈장치료제를 입원 후 사흘 안에 처방받은 환자들의 사망률이 감소하고 상태가 호전됐다고 밝혔다.
FDA는 지금까지 코로나19 환자 7만명이 혈장치료제를 처방받았으며, 이 중 2만명을 상대로 분석한 결과 치료제의 안전성을 확인했다고 말했다.
FDA는 80세 이하 환자에서 혈장치료제의 효과가 더 크게 나타났다고 덧붙였다.
피터 마크스 FDA 생물의약품 평가연구 센터장은 “우려되는 안전 문제는 보이지 않았다”고 말했다.
이와 관련, 도널드 트럼프 미국 대통령도 이날 오후 브리핑에서 코로나19 혈장치료에 대한 FDA의 긴급승인을 발표할 예정이라고 언론들이 보도했다.
워싱턴포스트(WP)는 당국자를 인용, 코로나19 백신과 치료제 확보를 대선 승리의 관건으로 보고 있는 트럼프 대통령이 반전을 모색하기 공화당 전당대회 전날 이러한 발표를 하는 것이라고 보도했다.
트럼프 대통령은 혈장치료의 긴급 승인이 전당대회의 하이라이트가 될 것을 기대하고 있다고 WP는 전했다.
그러나 혈장치료의 효과에 대해서는 아직 찬반양론이 있다. 혈장이 에볼라를 비롯한 전염병 치료에 오랫동안 사용된 건 사실이다. 그러나 코로나19 치료에도 효과가 있는지 엄정한 임상시험 결과가 나온 것이 아니어서 유망하기는 해도 확실하지는 않다는 것이다.
혈장 치료는 회복기 환자의 혈장을 추출해 다른 환자에게 주입하는 방식으로, 메르스와 사스 사태 당시에도 혈장 치료제가 사용된 적이 있다.
지난 4월 미국 내에서 코로나19 상황이 가장 심각했던 뉴욕주에서도 중증 환자들에 대해 혈장 치료제를 사용했었다. 지금까지 미국에서만 약 7만명의 환자가 혈장치료를 받은 것으로 추산된다.
그러나 전문가들은 혈장 치료의 효능을 증명하는 데이터가 부족하다고 지적해 왔다. 정치전문매체 폴리티코는 “FDA는 혈장치료의 효과에 대한 증거가 약하다는 전문가들의 우려에 따라 그동안 긴급 승인을 미뤄왔었다”고 지적했다.

[AFP=연합뉴스 자료사진]